Wo die Geschichte der Chromatographie anfängt, liegt im Dunkeln. Denn auch in der Natur spielen sich Vorgänge ab, bei denen sich ein chemisches Gemisch in seine Einzelkomponenten auftrennt, während es eine aus unterschiedlichen Materialien bestehende Umgebung durchläuft. Um 1900 beobachtete beispielsweise der amerikanische Geo-Chemiker David Talbot Day (1859 – 1925), dass die Komponenten von Rohöl, wenn sie durch bestimmte poröse oder feinkörnige Gesteine wie Kalk sickern, sich in langkettige, zyklische und aromatische Kohlenwasserstoffe sortieren können und dabei unterschiedlich farbige Banden im Gestein hinterlassen.
Ferdinand Runges „Chemische Wappen“
Die Auftrennung von Farbstoff-Mischungen dient bis heute als Spiel zur Unterhaltung: auf ein Stück Lösch- oder Fließpapier wird ein Tintenklecks getupft und sodann auf die gleiche Stelle ein paar Tropfen verdünnter Alkohol, um dann zu beobachten, wie das Papier die Flüssigkeit aufnimmt und die unterschiedlichen Farbstoffe, aus denen die Tinten gewöhnlich zusammengesetzt sind, ringförmig vom Ausgangspunkt nach außen wandern und die Phantasie anregende Bilder hinterlassen. Ähnliche Bilder lassen sich auch aus Pflanzenextrakten mit Benzin als „Entwicklerflüssigkeit“ auf saugfähigem Papier erzeugen.
Einer, der schon frühzeitig mögliche Anwendungen solcher Bilder, erkannte, war der deutsche Chemiker Friedlieb Ferdinand Runge (1794 – 1867), der sie als „Bindungen, die durch chemische Wechselwirkung entstehen“ erklärte und 1855 in seiner Schrift „Der Bildungstrieb der Stoffe, veranschaulicht in selbständig gewachsenen Bildern” ausführlich beschrieb.
Bei diesem wird ein Tropfen der gelösten Probe mit einem spezifischen Reagenz auf einem Stück Fließpapier zusammengebracht, wobei eine Farbänderung die Anwesenheit eines bestimmten Stoffs anzeigt.
Der allgemein bekannte Säure-Basen-Test mittels pH-Papier – Fließpapierstreifen, die mit einem Säure-Basen-Farbindikator imprägniert sind – ist solch ein Tüpfel-Test zur pH-Messung. Es blieb dem österreichischen Chemiker Fritz Feigl (1891 – 1971) vorbehalten, den simplen Tüpfel-Test zu einer analytischen Schnellmethode weiter zu entwickeln, die in vielen chemisch-technischen Laboratorien nach wie vor ihre Berechtigung hat.

Indem Runge seine „Chemischen Wappen“ auf Fließpapier nicht nur aus Farbstoffgemischen mit unterschiedlichen Lösemitteln entwickelte und den Einfluss der Solvents auf die Bildung der Farbmuster beobachtete, sondern in gleicher Weise auch chemische Reagenzien auf Stoffe einwirken ließ, konnte er beim Vergleich mit unbekannten Stoffen bereits Rückschlüsse auf deren Zusammensetzung ziehen. Von daher können Runges „Chemische Wappen“ auch als Vorläufer der Ringchromatographie angesehen werden, eine heute nur noch wenig gebräuchliche Variante der Papierchromatographie.
Zu den Ersten, die den Mechanismus dieses Trenn-Effekts untersuchten, zählten im Jahre 1861 der deutsch-schweizerische Chemiker und Physiker Christian Friedrich Schönbein (1791 – 1868) und sein um viele Jahre jüngerer Kollege, der schweizer Chemiker Christoph Friedrich Goppelsroeder (1837 – 1919). Sie beobachteten die Diffusion von wässerigen Farbstofflösungen in Papier und anderen saugfähigen Materialien und führten Unterschiede in den Wanderungsgeschwindigkeiten auf die Kapillarwirkung zurück.
Von der Farb-Schrift zur Aufreinigung von Naturstoffen: Die erste Chromatographie-Säule
Die Chromatographie als taugliches Verfahren zur Auftrennung von Stoffen beginnt erst mit den Arbeiten des in Italien geborenen, russischen Botanikers Michail Semjonowitch Tswett (1872 – 1919), der im Jahr 1901 eine Methode beschrieb, um pflanzliche Farbstoffe voneinander zu trennen.
Dabei wandert das hydrophile, grüne Chlorophyll langsamer durch die Carbonatschicht als die weniger hydrophilen, gelb-orange gefärbten Carotinoide, sodass sich die Farbstoffe an unterschiedlichen Stellen der Säule anreicherten. Damit war Tswett als erstem die Auftrennung von natürlichen Farbstoffen gelungen.
Da Tswett im Russischen „Farbe“ bedeutet, hat er sich mit der von ihm 1906 aus dem Griechischen hergeleiteten Wortschöpfung „Chromatographie”, die frei am besten mit „farbig schreiben“ übersetzt werden kann (griech.: χρομα = Farbe und γραφειν = schreiben), ein bleibendes Denkmal gesetzt.
Vorerst jedoch blieb die Tswett‘sche „Chromatographische Adsorptionsanalyse“, wie er sie selbst nannte, weitgehend unbekannt, da er ausschließlich auf Russisch publiziert hatte. Auch die Wirkmechanismen für die Stofftrennung waren längst noch nicht geklärt. So versuchte dann auch der deutsch-jüdische Biochemiker Richard Willstätter (1872 – 1942) am Kaiser-Wilhelm-Institut für Chemie in Berlin Anfang des 20. Jahrhunderts vergebens, Chlorophyll aus Pflanzenextrakten zu isolieren. Stattdessen fand er in der Papier-Chromatographie – der Chromatographie, die saugfähiges Papier als feste Phase nutzt – ein Trennverfahren, mit dem er erfolgreicher war und ihm half, die chemische Summenformel des Chlorophylls zu ermitteln. Dafür erhielt er im Jahr 1915 den Nobelpreis für Chemie.
Die von Tswett beschriebene Säulenchromatographie fand erst in den 1930er Jahren größere Verbreitung, nachdem sie vor allem von den deutschen Biochemikern Edgar Lederer (1908 – 1988) und Richard Kuhn (1900 – 1967) in Heidelberg zu einer handhabbaren Labormethode weiter entwickelt worden war.
Die Chromatographie wird zum Standard in verschiedenen Fachgebieten
Den endgültigen Durchbruch der Chromatographie brachte das Verständnis des Mechanismus der Auftrennung durch die Arbeiten der beiden britischen Chemiker Archer John Porter Martin (1910 – 2002) und Richard Laurence Millington Synge (1914 – 1994) in den 1940er Jahren. Durch Rückgriff auf Erfahrungen bei der Flüssig-Extraktion fanden sie heraus, dass die chromatographische Auftrennung durch die unterschiedliche relative Verteilung der Stoffe zwischen stationärer und mobiler Phase erfolgt.
Sie wurde schon bald eingesetzt, um die Sequenzen von Peptiden zu entschlüsseln und so einen der Grundsteine der modernen Biochemie und Molekularbiologie zu legen.
Größenausschluss-Chromatographie
Die Größenausschluss-Chromatographie, die je nach Lösungsmittel auch als Gel-Permeations-Chromatographie oder Gel-Filtrations-Chromatographie bezeichnet wird, beruht, wie der Name besagt, auf einem Trennmechanismus nach Molekülgröße.
Die Analyten werden nach ihrer Größe getrennt, indem sie ein poröses Gel durchlaufen müssen. Kleine Moleküle können leichter in die Gelpartikel eindringen, wodurch sie einen längeren Weg zurücklegen müssen und später eluiert werden als größere. Daher ist diese Methode für die Analytik von Kunststoffen, bei der sich Stoffe eher durch Größe als durch ihre Chemie voneinander unterscheiden, besonders geeignet.
Hochleistungsflüssig-Chomatographie
Für große Moleküle, wie sie in der in der Bio- und Naturstoffchemie vorkommen, kam eine andere Weiterentwicklung der Verteilungschromatographie zum Einsatz: Die Hochdruck-Flüssigkeits-Chromatographie (HPLC), bei der das Trennverfahren beschleunigt wird. Maßgeblich dafür sind der hohe Druck bis 400 bar und der Einsatz sehr kleiner Partikel als stationäre Phase, die eine hohe Oberfläche bieten.
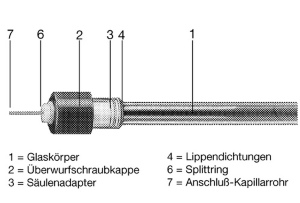
Für die HPLC benötigte Peripherie muss ebenso hohen Ansprüchen an die Druckbeständigkeit und chemische Inertheit genügen. So kommen als Schlauchleitungen besonders druckbeständige PEEK-Schläuche oder Titan- und Edelstahlkapillaren zum Einsatz, die mit Hilfe von Kapillar-Verbindern untereinander verbunden werden und den Anschluss an Säulen, Detektoren und andere Geräte erlauben.
Die Hochdruck-Technik, die der Säulenchromatographie zu höherer Leistung verhilft, ist aber nicht nur für die Auftrennung nach Hydrophobizität anwendbar, sondern hilft auch bei der Trennung nach anderen Molekül-Eigenschaften wie Größe, Ladung, oder Affinität zu einem bestimmten.
Dünnschischt-Chromatographie
Die Papierchromatographie von Willstätter wurde durch eine weitere, leistungsfähige Methode abgelöst: die Dünnschicht-Chromatographie. Das auf Arbeiten der beiden weitgehend unbekannt gebliebenen Russen N. A. Izmailov und M. S. Shraiber beruhende Verfahren aus dem Jahre 1938 wurde Anfang der 1960er Jahre von dem deutschen Chemiker und Pharmazeuten Egon Peter Gustav Stahl (1924 – 1986) in Zusammenarbeit mit den Firmen Merck (Darmstadt) und Degussa (Heidelberg) als ein nahezu universelles, analytisches Trennverfahren samt notwendiger technischer Ausrüstung für nichtflüchtige Stoffe etabliert.
Die Dünnschicht-Chromatographie ist technisch eine einfach und schnell durchführbare Methode. Statt Papier werden als stationäre Phase vorzugsweise Silicagele verwendet, aber auch Aluminiumoxide und modifizierte Cellulosen. Die stationäre Phase wird in einer dünnen Lage mit einem inerten Haft- und Bindemittel, wie Gips, auf einem flachen Träger, meist eine Glasplatte, aufgetragen und danach getrocknet.
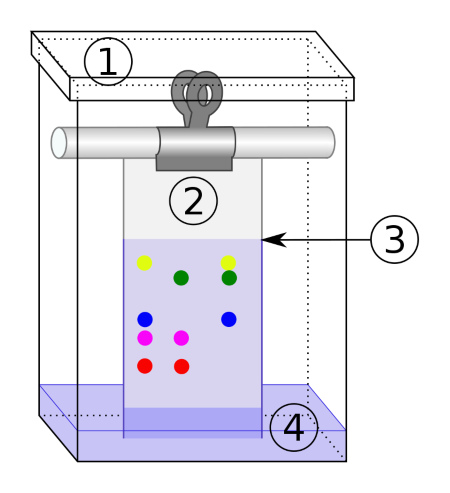
Die Proben werden, wie auch bei der Papierchromatographie, auf die trockene, feste Phase aufgetragen und die Platte sodann deutlich unterhalb der Auftragstelle senkrecht in einem geschlossenen Trog in das Elutionsmittel eingetaucht. Die Kapillarkräfte bewirken das Aufsteigen des Elutionsmittels in die feste Phase und damit die Auftrennung der Stoffe entsprechend ihres unterschiedlichen Adsorptions-Desorptionsverhaltens gegenüber der festen Phase.
Gaschromatographie
Basierend auf der Verteilungs-Chromatographie setzten die deutsche Physiko-Chemikerin Erika Cremer (1900 – 1996) und ihr Doktorand Fritz Prior (1921 – 1996) Ende der 1940er Jahre Gase, wie Helium oder Stickstoff, als mobile Phase statt einer Flüssigkeit ein und als stationäre Phase eine hochsiedende, viskose Flüssigkeit auf porösem, inerten Trägermaterial, wie Silikonöle auf Kieselgel. Ihre fundamentalen Arbeiten mündeten in ein neuartiges Säulen-Trennverfahren für gasförmige und unzersetzt verdampfbare Stoffe, die Gas-Chromatographie.
Ihre technische Weiterentwicklung zu einem leistungsfähigen Laborverfahren ist vor allem mit den Namen der britischen Chemiker Archer John Porter Martin (1910 – 2002) und Anthony Trafford James (1922 – 2006) eng verbunden. Zeitgleich wurden in den 1950er Jahren auch dazu kompatible Detektoren, wie der Wärmeleitfähigkeits-Detektor, der Flammen-Ionisations-Detektor, der Elektronen-Einfang-Detektor und schließlich auch massenspektrometrische Detektoren entwickelt, was zu der Verbreitung der Gaschromatographie als analytische und mikro-präparative Standardmethode entscheidend beitrug.
Ionenaustausch-Chromatographie
Die Ionenaustausch- oder Ionen-Chromatographie trennt geladene Moleküle, einschließlich Nukleinsäuren und Proteine, nach ihrem isoelektrischen Punkt. Je nach Ladung der zu trennenden Substanzen unterscheidet man zwischen Anionen- und Kationen-Austausch-Chromatographie. Das Prinzip beruht darauf, dass zu trennende Moleküle ionisch an eine entgegengesetzt geladene mobile Phase binden und dann durch die Gegenionen aus dem Elutionsmittel bei einem passendem pH oder passender Ionenstärke wieder eluiert werden – also ein Ionenaustausch stattfindet.
Bei der Anionen-Austausch-Chromatographie binden negativ geladene Moleküle, wie etwa Nucleinsäuren oder Proteine ionisch an eine positiv geladene mobile Phase, zum Beispiel an einem Diethyl-Aminoethyl-Harz, während bei der Kationen-Austausch-Chromatographie positiv geladene Ionen, wie etwa Metall-Kationen, an eine negativ geladene mobile Phase binden. Eine der ersten Anwendungen dieser Methode war in den 1940er Jahren die Auftrennung der wegen ihrer chemischen Ähnlichkeit nur schwer zu unterscheidenden Selten-Erdmetalle. Die Ionenaustausch-Chromatographie wird auch heute noch für die Gewinnung reiner Seltener Erdmetalle eingesetzt, die für die gesamte Mikroelektronik unentbehrliche Grundstoffe sind.
Affinitäts-Chromatographie
Breite Anwendung in den Biowissenschaften findet die Affinitäts-Chromatographie, die in den 1960er Jahren von dem spanisch-amerikanischen Pharmakologen Pedro Martin Cuatrecasas (1936 – ) und dem israelischen Biochemiker Meir Wilchek (1935 – ) entwickelt wurde. Sie beruht auf den Wechselwirkungen von Biomolekülen mit ihren Liganden, wie etwa zwischen Enzym und Substrat oder zwischen Antikörper und Antigen. Das Biomolekül bindet an seinen immobilisierten Liganden und wird durch gezielte Änderung von Bedingungen wie pH-Wert, Salzkonzentration oder Zugabe von kompetierenden Liganden wieder eluiert.

Diese Methode wird auch oft zur Aufreinigung von genetisch markierten Proteinen verwendet, die an einem „tag“ (engl.: tag = Markierung), wie etwa Histidin- oder Glutathion-S-Transferase gebunden sind, der die Wechselwirkung mit einer spezifischen festen Phase ermöglicht. Mit der Affinitätschromatographie ist die sehr spezifische Aufreinigung von Biomolekülen in komplexen Stoffgemischen möglich. Da sie auch für die Aufreinigung von Impfstoffen verwendet wird, haben die meisten von uns wohl schon mal von der Leistungsfähigkeit dieser Technik im direkten Kontakt profitiert.
Ferdinand Runges Vermächtnis heute
Vor über 150 Jahren präsentierte Ferdinand Runge seine chemischen Wappen und selbstständig gewachsenen Bilder der Öffentlichkeit, deren Entstehen er mit chemischen Wechselwirkungen erklärte. Dass er damit am Anfang einer stürmischen Entwicklung der Stofftrennungen stand, wird ihm wohl kaum bewusst geworden sein.
Aber nachfolgende Wissenschaftler-Generationen griffen seine grundlegenden Gedanken auf, entwickelten sie weiter und so zeigt sich die Chromatographie heutzutage in vielen technisch ausgereiften Varianten zur Trennung von Stoffen sowohl im Mikro-Maßstab zur Analyse von Stoffgemischen als auch im Makro-Maßstab zur Reindarstellung von Stoffen. Ohne den Einsatz dieser modernen chromatographischen Trenn- und Reinigungsverfahren müssten wir auf manches Liebgewonnene oder auch Lebensnotwendige verzichten, es gäbe weder Handys noch spezifische Impf- und Arzneistoffe – und vieles andere wohl auch nicht.
Bild-Quellen: Beitragsbild | © sinhyu – stock.adobe.com Messung des pH-Werts | © Kim – stock.adobe.com Schematische Darstellung der Papier-Chromatographie | © Theresa Knott, CC BY-SA 3.0 <https://creativecommons.org/licenses/by-sa/3.0>, via Wikimedia Commons Hochdruckschläuche an der Pumpe eines HPLC Systems | © vladim_ka – stock.adobe.com
 Reichelt Chemietechnik Magazin
Reichelt Chemietechnik Magazin