HPLC steht für High Performance Liquid Chromatography, auf Deutsch Hochleistungsflüssigkeitschromatographie. Sie wird sowohl für präparative wie auch analytische Stofftrennungen eingesetzt. Besonders hilfreich ist die HPLC für die Biochemie bei der Präparation und Analyse von Stoffen mit hohen Molekulargewichten wie Proteinen.
Was ist Flüssigchromatographie?
Bei der Chromatographie handelt es sich um ein Trennverfahren, bei dem ein Stoffgemisch mit Hilfe von zwei Phasen, einer stationären und einer mobilen Phase, aufgetrennt wird. Wenn von Flüssigchromatographie die Rede ist, dann ist die stationäre Phase ein Feststoff, die mobile Phase eine Flüssigkeit. Sie wird als Eluent bezeichnet.
Die mobile Phase bewegt sich an der stationären Phase vorbei und das zu trennende Gemisch wird dabei entsprechend der Wechselwirkungen zwischen der jeweiligen Substanz und der stationären Phase in seinem Durchlauf verzögert und dadurch aufgetrennt.
Als stationäre Phase können verschiedene Stoffe dienen: Bei der Papierchromatographie sind dies spezielle Filterpapiere; bei Säulen- und Dünnschichtchromatographie werden meist Kieselgel oder Aluminiumoxid verwendet. Die mobilen Phasen reichen von unpolaren Lösungsmitteln, wie Hexan, bis zu polaren Lösungsmitteln, wie Wasser.
Wie funktioniert die HPLC?
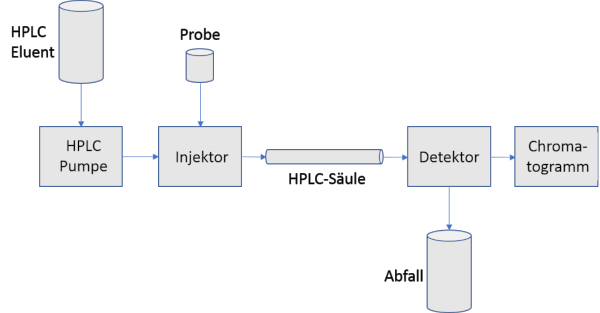
Die HPLC ist im Grunde eine technisch optimierte Säulenchromatographie. Bei diesem Trennverfahren drückt eine Pumpe kontinuierlich mit 50 – 400 bar den Eluenten, also die mobile Phase, möglichst pulsationsarm durch die Chromatographiesäule, die mit der festen stationären Phase gefüllt ist.
Wird am Säulenanfang eine Probe mit Hilfe eines Injektors eingespritzt, erfolgt die Auftrennung in der Säule. Ein nachgeschalteter Detektor misst ein zur eluierten Komponentenmenge proportionales Signal, um dieses anschließend als Graphik, dem sogenannten Chromatogramm, auszugeben und zu qualifizieren. Im Idealfall repräsentiert jeder Peak eines Chromatogramms eine Komponente des Stoffgemischs.

Gebräuchliche Detektoren sind zum Beispiel UV-Absorptions-, Brechungsindex- oder Fluoreszenz-Detektoren. Durch Rückführung von reinen, nicht mit Probe verunreinigten Eluenten, kann der Lösemittelverbrauch einer solchen Anlage deutlich gesenkt werden.
Im Unterschied zur einfachen Säulenchromatographie, die ohne Druck arbeitet, sind bei der Hochleistungsflüssigkeitschromatographie die Probenmengen wesentlich kleiner, die Elutionsgeschwindigkeit deutlich höher und die Trennleistung sehr viel besser.. Durch einen Säulenofen kann die HPLC-Säule zusätzlich beheizt werden, wodurch sich die Wechselwirkungsprozesse zwischen mobiler und stationärer Phase ändern und damit die Trennleistung der Säule beeinflussen.

Bei Geräten zur Ultrahochleistungsflüssigkeitschromatographie (UHPLC) werden noch kleinere Partikel und gleichzeitig noch kürzere und dünnere Säulen verwendet und somit die Trennleistung weiter optimiert.
Im Folgenden gehen wir kurz auf die üblichen Baugruppen einer HPLC ein:
- Probeninjektion
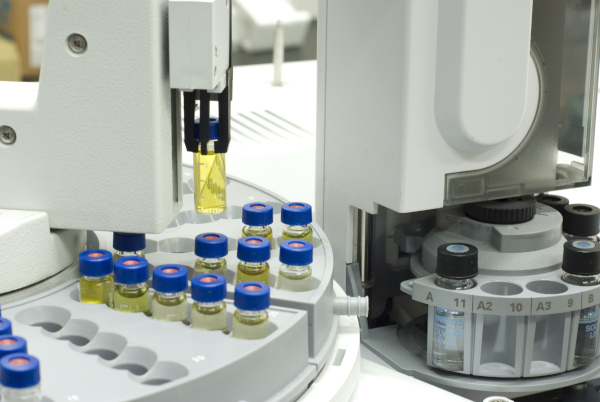
Die Injektion der gelösten Probe erfolgt üblicherweise mit Hilfe von Probenschleifen mit definiertem Volumen, in die die Probe zunächst eingeschleust wird. Ein Sechswegeventil ermöglicht nach Umschalten, dass der Eluent durch die mit der Probe geladenen Schleife fließt und dadurch die Probe auf der Säule aufgebracht wird.
Im Nieder- und Mitteldruckbereich ist auch die Probeninjektion mittels Dosierspritze möglich. Im Routinebetrieb reduziert ein Autosampler den manuellen Arbeitsaufwand. Die Injektionsvolumina sind vom Säulendurchmesser abhängig und liegen in der Regel bei nur 1 µl bis 2 ml.
- Chromatographiesäule
Da mit hohen Drücken bis 400 bar gearbeitet wird, werden Säulen aus dickwandigem Glas verwendet, das aus Sicherheitsgründen meist mit einem druckbeständigem Edelstahlrohr ummantelt ist. Hochdruckfeste Säulen aus Edelstahl können hingegen wegen der Empfindlichkeit vieler bioaktiver Stoffe gegenüber Schwermetallen für biochemische Arbeiten kaum eingesetzt werden. Gelegentlich kommen jedoch auch Säulen aus bioinertem Titan zum Einsatz. Die effektiven Innendurchmesser von HPLC-Säulen betragen im Regelfall nur wenige Millimeter.


- Stationäre Phase
HPLC-Säulen sind mit einem festen, aber porösen und druckbeständigem Material, meist einem funktionalisierten Kieselgel, dicht gepackt. Im Vergleich zur normalen Flüssigkeitschromatographie im Niederdruckbereich ist die Teilchengröße der stationären Phase bei der HPLC mit < 10 μm erheblich kleiner. Je kleiner die Partikel sind, desto höher ist die Trennleistung.
Die Trennung der Probe ist nach verschiedenen Prinzipien wie Adsorption-, Ionenaustausch- und Größenausschluss-Chromatographie möglich und eröffnet so eine vielseitige Bandbreite der möglichen Anwendungen.


Meist erfolgt die Trennung aufgrund der Polaritätsunterschiede zwischen mobiler und stationärer Phase. Man unterscheidet dabei zwischen Normalphasen-HPLC mit einer polaren stationären und einer unpolaren mobilen Phase (NP) und Umkehrphasen-HPLC (RP) mit entsprechend vertauschten Polaritäten.
Die Polaritäten der stationären und mobilen Phasen haben erheblichen Einfluss auf die Retentionszeit, die Laufzeit einer Substanz durch die Säule. Eine Substanz besitzt keine bzw. nur sehr schwache Wechselwirkungen mit einer unpolaren stationären Phase und hat deshalb eine kurze Retentionszeit.
Da die Normalphasen-HPLC jedoch schwieriger in der Handhabung ist, z. B. wegen Probleme durch Wasser im Lösemittel, ist heute die Umkehrphasen-HPLC die sehr viel öfter eingesetzte Methode.


- Mobile Phase
Bei der Auswahl des Eluents können Polaritätsübersichten beziehungsweise elutrope Reihen helfen. Für eine Vielzahl von Gemischen benötigt man Lösungsmittelgemische, mit denen gezielt die Polarität und damit auch die Elutionskraft eingestellt werden kann. Mittels elektronisch gesteuerter Mischer für die Lösungsmittel lassen sich Polaritätsgradienten des Eluenten einstellen.
Anwendungsbreite einer Hochleistungsflüssigkeitschromatographie
- Analytisch
Die analytische Identifizierung einer Substanz erfolgt meist durch Vergleich der Retentionszeiten der Probe mit derjenigen eines Vergleichsstoffes. Man kann beispielsweise Probe und Vergleich mischen und zusammen injizieren, es sollte sich dann ein vergrößerter Peak ergeben. Wird jedoch ein zweiter Peak eluiert, sind Probe und Vergleichsstoff nicht identisch. Durch Wiederholen der Analyse nach Wechseln der mobilen Phase kann weitestgehend sichergestellt werden, dass die Peaks sich nicht nur zufällig überlagert haben.
Noch höhere Sicherheit bringt das Wechseln der stationären Phase (z. B. Umkehrphasen- statt Normalphasen-HPLC). Hundertprozentige Sicherheit erhält man allerdings nur die qualitative Analyse der Substanz zum jeweiligen Signal. Dies kann auch mit spezifischen nachgeschalteten Detektoren, wie Massenspektroskopie oder Diodenarray, mit dem das gesamte UV/Vis-Spektrum eines Signals aufgezeichnet wird, erreicht werden.
- Präparativ
Genau wie eine normale Säulenchromatographie, lässt sich eine HPLC auch zur Reinigung von Substanzen, wie beispielsweise von pharmazeutischen Produkten oder biologischer Proben, verwenden. In der Regel werden dafür Säulen mit größeren Innendurchmessern benötigt, weil die Mengen der aufzureinigenden Proben meist um ein Vielfaches größer sind als bei analytischen Trennungen.
Bedeutung in der Biochemie
Durch die Vielzahl der verschiedenen Trennprinzipien und durch unterschiedlichste Detektoren ist die Hochleistungsflüssigkeitschromatographie ein sehr vielseitiges und potentes Analysetool, vor allem auch in der Biochemie, wo Gemische aus Biopolymeren, wie Nukleinsäuren, Aminosäuren, Peptide oder Enzyme, identifiziert werden müssen. Bei entsprechender Dimensionierung der Säulen ist die HPLC auch für präparative Trennungen zur Reindarstellung von Stoffen aus Gemischen geeignet. Sie ist damit insbesondere für das biochemische Labor unverzichtbar geworden.
Auch für medizinische Zwecke, wie die Bestimmung des Vitamin D-Gehalts im Blut, wird die Hochleistungsflüssigkeitschromatographie heute eingesetzt.
Weitere typische Anwendungen beinhalten die Analyse von Polymeren, Wirkstoffen und Schadstoffen, Reinheitskontrollen oder Mengenbestimmungen, z. B. von Wirkstoffen in biologischen Proben. Auch in der Trinkwasserkontrolle wird HPLC-Analytik heute standardmäßig verwendet.
 Reichelt Chemietechnik Magazin
Reichelt Chemietechnik Magazin
